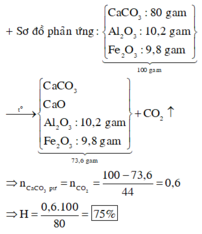
Một loại đá vôi chứa 85% CaCO3 và 15% tạp chất không bị phân hủy ở nhiệt độ cao . Khi nung một lượng đá vôi đó thu được một chất rắn có khối lượng bằng 70% khối lượng đá trước khi nung
a, Tính hiệu suất quá trình phản ứng
b, Tính thành phần % khối lượng CaO trong chất rắn sau khi nung